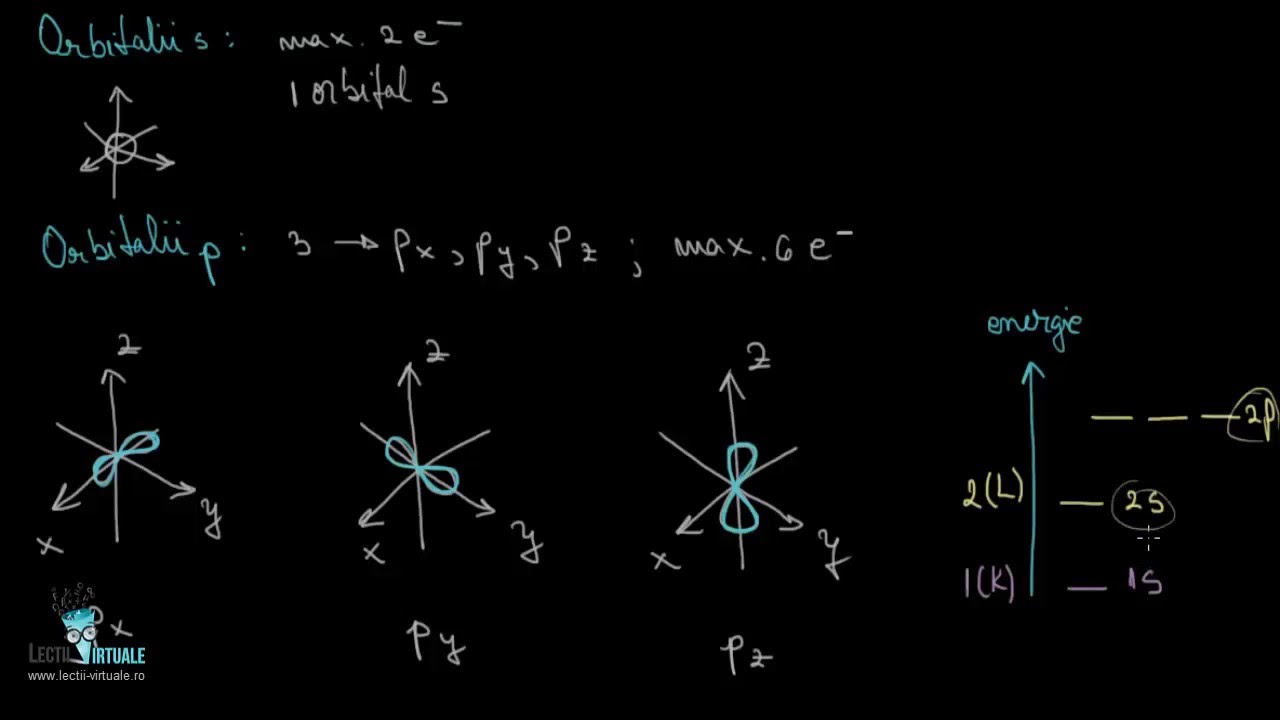Repartizarea Electronilor Pe Straturi Exemple
Modele digitale ale structurii atomilor completate.
Repartizarea electronilor pe straturi exemple. Numărul de protoni neutroni electroni repartizarea electronilor pe straturi. Configuratia electronica a elementelor. Electronii sunt situati pe 7 straturi numerotate de la nucleu spre exterior cu cifre de la 1 la 7 sau cu litere de la k la q. Reguli de ocupare cu electroni a straturilor substraturilor si orbitalilor.
Structura învelişului de electroni. Principiul de excluziune al lui pauli regula lui hund. Fișă de caracterizare a elementului chimic completată. Principiul stabilității al minimei energii.
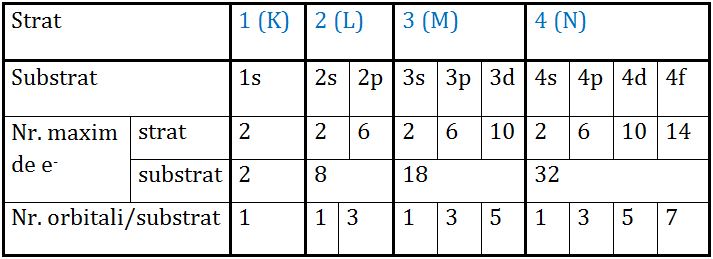
Deşi sunt 7 straturi k l m n o p q se cunoaşte repartizarea electronilor doar pe primele 4 k l m n. Acest articol despre un element chimic este un ciot. Substraturi straturi electronice publicat. Intr un orbital incap maxim 2 electroni cu spin opus.
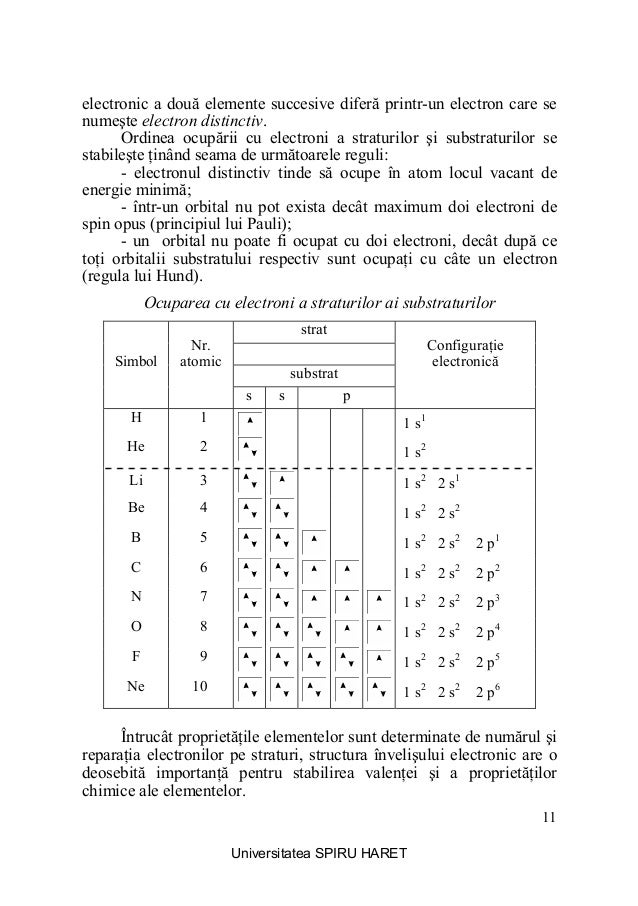
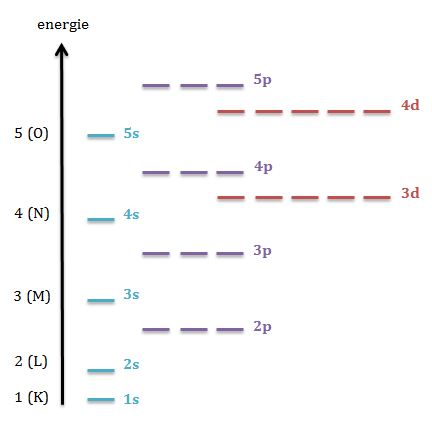
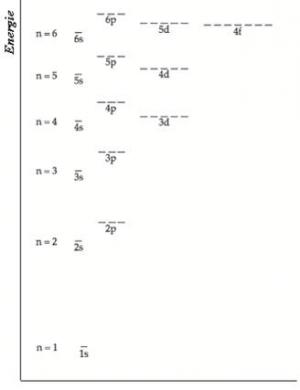
Ex invelisul de electroni k cu numar cuantic principal n 1 este nivelul de energie cel mai slab corespunde un anumit numar de orbite rezulta ca numarul maxim de electroni dintr un substrat este bine determinat dupa cum. Repartizarea electronilor pe straturi şi substraturi. Straturile 5 6 7 sunt straturi parţial ocupate cu electroni pentru că nu toate substraturile acestor straturi sunt ocupate de electroni. Configura tia electronica reprezinta repartizarea electronilor pe straturi substraturi si orbitali.
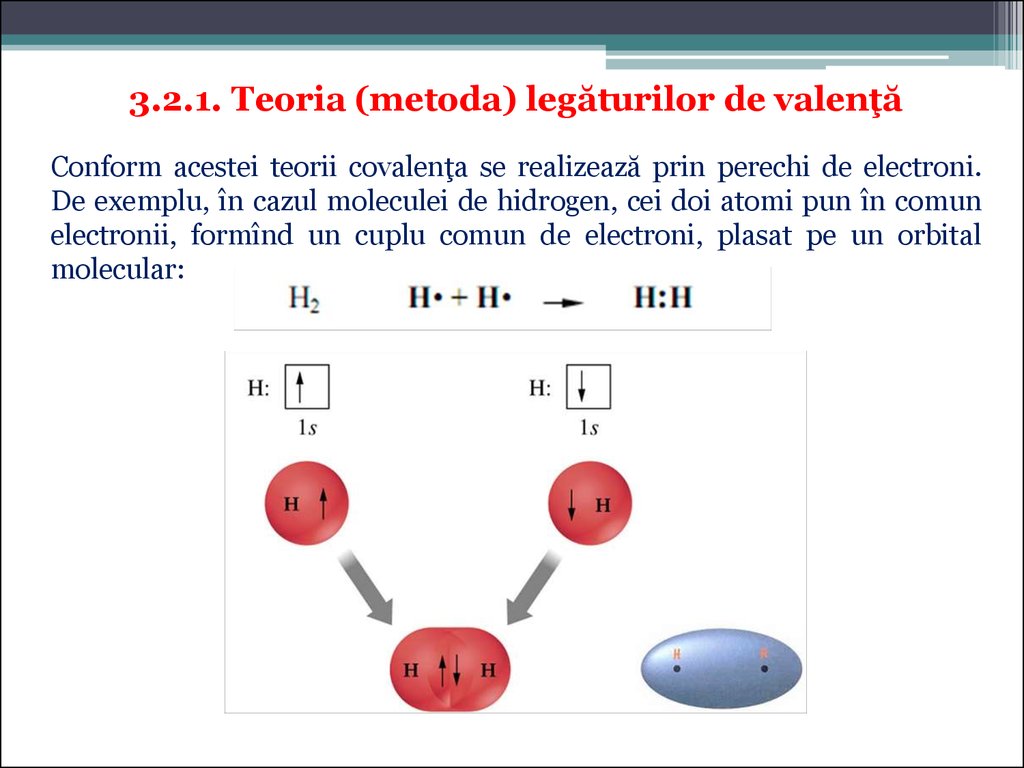
Z 6 a 12 atomul de carbon c are z 6 deci cuprinde 6 protoni în nucleu și 6 electroni în învelișul electronic. Ocuparea cu electroni a orbitalilor atomici are la bază ocuparea orbitalilor atomici cu electroni se sprijină pe 3 principii de bază. Atomul de hidrogen are un singur electron care graviteaza in jurul nucleului si va ocupa orbita lul de energie cea mai joasa din primul strat k adica orbitalul 1s acelasi electron functie de aportul de energie radiativa din exterior poate ocupa oricare orbital din nivelele de. Maxim de electroni care pot ocupa un strat 2n 2 n nr.
Se stie ca la fiecare nivel de energie valoarea permisa a energiei unui sistem cuantic atom molecula etc raportata la o anumita stare ca stare fundamentala. Electronii de pe ultimul nivel ii imprima atomului proprietatile chimice si culoarea comportamentul electronilor de pe ultimul nivel se caracterizeaza drept proprietate chimică a elementului.